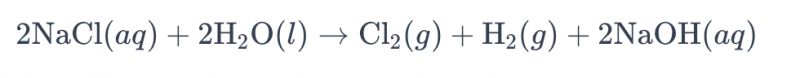ຂະບວນການແຍກສານລະລາຍນ້ຳເຄັມໂດຍໃຊ້ເອເລັກໂຕຣດໄທທານຽມເພື່ອຜະລິດຄລໍຣີນມັກຈະຖືກເອີ້ນວ່າ "ການແຍກສານນ້ຳເຄັມດ້ວຍເອເລັກໂຕຣດ". ໃນຂະບວນການນີ້, ເອເລັກໂຕຣດໄທທານຽມຖືກນຳໃຊ້ເພື່ອອຳນວຍຄວາມສະດວກໃຫ້ແກ່ປະຕິກິລິຍາອົກຊີເດຊັນຂອງໄອອອນຄລໍໄຣດ໌ໃນນ້ຳເຄັມ, ເຊິ່ງນຳໄປສູ່ການສ້າງອາຍແກັສຄລໍໄຣນ. ສົມຜົນທາງເຄມີໂດຍລວມສຳລັບປະຕິກິລິຍາມີດັ່ງນີ້:
ໃນສົມຜົນນີ້, ໄອອອນຄລໍໄຣດ໌ຈະຜ່ານການຜຸພັງຢູ່ທີ່ຂົ້ວບວກ, ເຊິ່ງສົ່ງຜົນໃຫ້ເກີດອາຍແກັສຄລໍໄຣດ໌, ໃນຂະນະທີ່ໂມເລກຸນນໍ້າຖືກຫຼຸດລົງຢູ່ທີ່ຂົ້ວລົບ, ເຊິ່ງເຮັດໃຫ້ເກີດອາຍແກັສໄຮໂດຣເຈນ. ນອກຈາກນັ້ນ, ໄອອອນໄຮດຣອກໄຊດ໌ຈະຜ່ານການຜຸພັງຢູ່ທີ່ຂົ້ວບວກ, ເຊິ່ງປະກອບເປັນອາຍແກັສໄຮໂດຣເຈນ ແລະ ໂຊດຽມໄຮດຣອກໄຊດ໌.
ການເລືອກເອເລັກໂຕຣດໄທທານຽມແມ່ນຍ້ອນຄວາມຕ້ານທານການກັດກ່ອນ ແລະ ການນຳໄຟຟ້າທີ່ດີເລີດຂອງໄທທານຽມ, ຊ່ວຍໃຫ້ມັນສາມາດເກີດປະຕິກິລິຍາໄດ້ຢ່າງໝັ້ນຄົງໃນລະຫວ່າງການແຍກດ້ວຍໄຟຟ້າໂດຍບໍ່ມີການກັດກ່ອນ. ສິ່ງນີ້ເຮັດໃຫ້ເອເລັກໂຕຣດໄທທານຽມເປັນທາງເລືອກທີ່ເໝາະສົມສຳລັບການແຍກດ້ວຍໄຟຟ້າຂອງນ້ຳເຄັມ.
ການແຍກນ້ຳເຄັມດ້ວຍໄຟຟ້າໂດຍທົ່ວໄປແລ້ວຕ້ອງການແຫຼ່ງພະລັງງານຈາກພາຍນອກເພື່ອສະໜອງພະລັງງານໃຫ້ກັບປະຕິກິລິຍາເອເລັກໂຕຼໄລຕິກ. ແຫຼ່ງພະລັງງານນີ້ມັກຈະເປັນແຫຼ່ງພະລັງງານກະແສໄຟຟ້າໂດຍກົງ (DC) ເພາະວ່າປະຕິກິລິຍາເອເລັກໂຕຼໄລຕິກຕ້ອງການທິດທາງການໄຫຼຂອງກະແສໄຟຟ້າທີ່ສະໝໍ່າສະເໝີ, ແລະແຫຼ່ງພະລັງງານ DC ສາມາດສົ່ງກະແສໄຟຟ້າໄດ້ໃນທິດທາງທີ່ຄົງທີ່.
ໃນຂະບວນການ electrolyze ນ້ຳເຄັມເພື່ອຜະລິດອາຍແກັສ chlorine, ແຫຼ່ງພະລັງງານ DC ແຮງດັນຕ່ຳແມ່ນຖືກນຳໃຊ້ທົ່ວໄປ. ແຮງດັນຂອງແຫຼ່ງພະລັງງານແມ່ນຂຶ້ນກັບເງື່ອນໄຂປະຕິກິລິຍາສະເພາະ ແລະ ການອອກແບບອຸປະກອນ, ແຕ່ໂດຍທົ່ວໄປແລ້ວຢູ່ໃນລະຫວ່າງ 2 ຫາ 4 ໂວນ. ນອກຈາກນັ້ນ, ຄວາມເຂັ້ມຂອງກະແສໄຟຟ້າຂອງແຫຼ່ງພະລັງງານແມ່ນຕົວກຳນົດທີ່ສຳຄັນທີ່ຕ້ອງໄດ້ກຳນົດໂດຍອີງໃສ່ຂະໜາດຂອງຫ້ອງປະຕິກິລິຍາ ແລະ ຜົນຜະລິດທີ່ຕ້ອງການ.
ສະຫຼຸບແລ້ວ, ການເລືອກແຫຼ່ງພະລັງງານສຳລັບການແຍກນ້ຳເຄັມດ້ວຍໄຟຟ້າແມ່ນຂຶ້ນກັບຄວາມຕ້ອງການສະເພາະຂອງການທົດລອງ ຫຼື ຂະບວນການອຸດສາຫະກຳເພື່ອຮັບປະກັນປະຕິກິລິຍາທີ່ມີປະສິດທິພາບ ແລະ ການບັນລຸຜະລິດຕະພັນທີ່ຕ້ອງການ.
ເວລາໂພສ: ມັງກອນ-16-2024